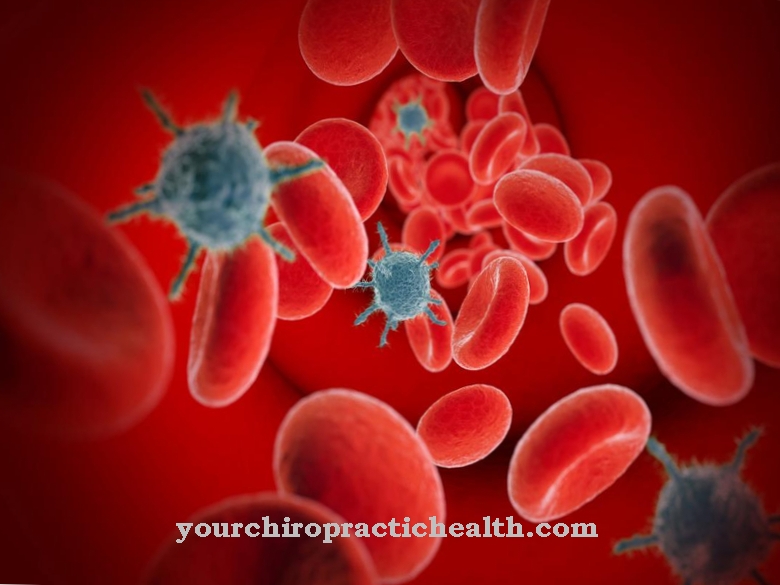
Dintre presiune osmotica corespunde presiunii care este prezentă în solvent pe partea mai concentrată a unei membrane semipermeabile sau selectiv permeabile. Presiunea conduce fluxul de solvent prin membrană și dictează direcția sa. Bolile legate de presiunea osmotică sunt, de exemplu, scăderea rezistenței la presiune a celulelor sanguine.
Ce este presiunea osmotică?

Cu termenul de presiune osmotică, medicamentul descrie presiunea fiziologică care permite osmoza. Osmoza corespunde fluxului direcționat de particule moleculare prin straturi de separare semipermeabile sau permeabile selectiv. Aceasta înseamnă că osmoza este un transport esențial al substanțelor în corpul uman.
Presiunea osmotică este principala cerință pentru acest proces de transfer de masă. Moleculele dizolvate într-un solvent determină presiunea osmotică pe partea interfeței cu o concentrație mai mare. Raporturile de presiune rezultate conduc fluxul solventului prin membrana respectivă. În acest fel, solventul se deplasează din lateral cu concentrația mai mică de particule prin membrană și astfel curge în lateral cu concentrația mai mare pe care există presiunea osmotică. Particulele moleculare în sine nu pot trece prin membrana semipermeabilă sau permeabilă selectiv.
Funcție și sarcină
Presiunea osmotică depinde de raporturile de concentrație ale două soluții, care sunt situate pe laturi diferite ale unei membrane semipermeabile sau selectiv permeabile. Deși există o presiune osmotică pe partea concentrată inferioară, presiunea este întotdeauna mai mare pe partea mai concentrată a solutului.
În corpul uman, apa curge în celulele individuale din interstițiu. Acest influx apare de la o parte cu o concentrație mai mică la o parte cu o concentrație mai mare. Celulele au o anumită presiune internă. Această presiune este cunoscută și sub denumirea de turgor. Fluxul continuă până când turgorul din celule a atins același nivel cu presiunea osmotică. Prin urmare, presiunea existentă în interior și presiunea care acționează la exterior sunt echivalente la sfârșitul intrării.
Presiunea osmotică poate fi măsurată și calculată. În principiu, aceleași legi ale fizicii se aplică în soluții lichide diluate ca în gazele ideale. Din acest motiv, presiunea osmotică este întotdeauna proporțională cu temperatura absolută în fiecare caz. În plus, există o proporționalitate între concentrația molară a substanței dizolvate particulare și nivelul presiunii osmotice.Presiunea depinde în primul rând de numărul de particule moleculare din substanța dizolvată.
Într-o soluție dintr-un mol de substanță în 22,4 litri de solvent, presiunea osmotică la temperaturi de 0 grade Celsius sau 273,15 Kelvin este 101.325 kPa. Legea lui Hoff a lui Van oferă aceste relații. Cu toate acestea, legea se aplică numai soluțiilor diluate sub o valoare de 0,1 M.
Analogia legilor gazelor ideale este următoarea: presiunea osmotică contracarează influxul de solvenți. Din acest motiv, fluxul de solvent se oprește imediat ce este atins echilibrul.
Presiunea osmotică a unei soluții poate fi determinată cu osmometre. Presiunea este măsurată fie static, după atingerea echilibrului, fie dinamic. Prin măsurarea dinamică, trebuie să se aplice presiune externă pe manometrul de ridicare pentru a întrerupe fluxul osmotic. Prin măsurarea presiunii se poate determina și masa moleculară medie a macromoleculelor.
Boli și afecțiuni
De exemplu, bolile legate de presiunea osmotică pot afecta celulele sanguine. Globulele roșii au o rezistență osmotică. Această rezistență osmotică a globulelor roșii este redusă în diferite boli. La fel cum multe boli sunt asociate cu o creștere a rezistenței osmotice. Pentru a recunoaște astfel de boli, se măsoară rezistența osmotică a eritrocitelor. Mai presus de toate, măsurarea permite diagnosticul bolilor care reduc rezistența.
Aceste boli includ, de exemplu, anemia celulelor sferoidale. Cu toate acestea, alte anemii hemolitice pot reduce, de asemenea, rezistența osmotică a globulelor roșii. Anemia hemolitică este un grup de boli asociate cu anemie datorată unei descompuneri crescute sau premature a eritrocitelor. Medicina numeste acest fapt hemoliza. Hemoliza este adesea asociată cu bolile subiacente. Ele pot fi cauzate de procese mecanice sau de dispoziție genetică. Pe lângă hemoliza fiziologică datorată vârstei eritrocitelor, o utilizare excesivă mecanică, cum ar fi înlocuirea valvei cardiace, deteriorarea termică cauzată de încălzire și deteriorarea osmotică poate determina descompunerea. În cazul deteriorării osmotice, soluțiile hiper- sau hipoosmolare sunt cauza reală a degradării.
Pentru a măsura rezistența osmotică, globulele roșii ale pacientului sunt plasate în tuburi cu concentrația de sare crescândă. Unul dintre tuburi conține apă aproape pură. Unul conține o concentrație de sare care este optimă pentru globulele roșii. După 24 de ore, celulele sanguine izbucnesc în apa pură. În tuburile cu o concentrație mai mare de sare, doar câteva dintre celulele sanguine tind să izbucnească. Dacă pacientul suferă de o boală cu scăderea rezistenței osmotice a celulelor sanguine, corpusculii izbucnesc chiar și în concentrații mai mari de sare și nu pot rezista la presiunea osmotică.
Rezistența osmotică poate fi, de asemenea, crescută. O creștere a rezistenței nu este specifică și poate fi rezultatul diferitelor boli. Exemple de boli cu rezistență osmotică crescută a globulelor roșii sunt talasemia, anemia cu deficit de fier și anemia celulelor secera. În plus, icterul și leziunile hepatice pot crește rezistența.










.jpg)