gluconeogeneză asigură noua sinteză a glucozei din piruvat, lactat și glicerină din organism. Acest lucru asigură furnizarea de glucoză a organismului în perioadele de foame. Tulburările de gluconeogeneză pot duce la hipoglicemie periculoasă.
Ce este Gluconeogeneza?

În timpul gluconeogenezei, glucoza este generată din nou din produsele de descompunere a proteinelor, a glucidelor și a metabolismului grăsimilor.
Reacțiile la gluconeogeneză au loc în principal în ficat și mușchi. Acolo glucoza sintetizată este apoi condensată în glucogen, o substanță de stocare care servește ca un depozit de energie pentru furnizarea rapidă de energie a celulelor nervoase, eritrocitelor și mușchilor. Prin gluconeogeneză, 180 până la 200 de grame de glucoză pot fi formate nou pe zi.
Gluconeogeneza poate fi privită ca reversul glicolizei (descompunerea glucozei) la piruvat sau lactat, deși trei etape de reacție trebuie înlocuite cu reacții de ocolire din motive energetice. Glicoliza produce piruvat (acid piruvic) sau, în condiții anaerobe, lactat (anion de acid lactic). Mai mult, acidul piruvic este format și din aminoacizi atunci când sunt descompuse. Un alt substrat pentru regenerarea glucozei este glicerina, care provine din descompunerea grăsimilor. Este transformat în dihidroxiacetona fosfat, care acționează ca un metabolit în lanțul de sinteză a gluconeogenezei pentru a acumula glucoză.
Funcție și sarcină
Se pune întrebarea de ce ar trebui să fie acumulată din nou glucoza dacă anterior a fost defalcat prin glicoliză pentru a genera energie. Trebuie remarcat însă că celulele nervoase, creierul sau eritrocitele sunt dependente de glucoză ca furnizor de energie.
Dacă consumurile de glucoză din organism sunt consumate fără a fi completate suficient de repede, apare o hipoglicemie periculoasă, care poate fi chiar fatală. Cu ajutorul gluconeogenezei, nivelul normal al glicemiei poate fi menținut constant chiar și în perioadele de foame sau în situații de urgență consumatoare de energie.
O treime din glucoza nou sintetizată este stocată sub formă de glucogen în ficat și două treimi în mușchii scheletului. Dacă vă este foame pentru o perioadă mai lungă de timp, nevoia de glucoză scade ușor, deoarece a doua cale metabolică este utilizarea corpurilor cetonice pentru a genera energie.
Rolul central în gluconeogeneză îl joacă acidul piruvic (piruvat) sau acidul lactic (lactat) format din acesta în condiții anaerobe. Ambii compuși sunt, de asemenea, produse de descompunere în timpul glicolizei (descompunerea zahărului).
În plus, piruvatul se formează și atunci când se descompun aminoacizii. În altă parte, glicerina din descompunerea grăsimilor poate fi, de asemenea, transformată într-un metabolit al gluconeogenezei și este încorporată în acest proces. În timpul gluconeogenezei, glucoza este produsă din nou din produsele de descompunere a metabolismului glucidelor, proteinelor și grăsimilor.
Mecanismele proprii de reglementare ale organismului asigură faptul că gluconeogeneza și glicoliza nu au loc în același timp. Odată cu creșterea glicolizei, gluconeogeneza este oarecum slăbită. Într-o fază de gluconeogeneză crescută, glicoliza este din nou redusă.
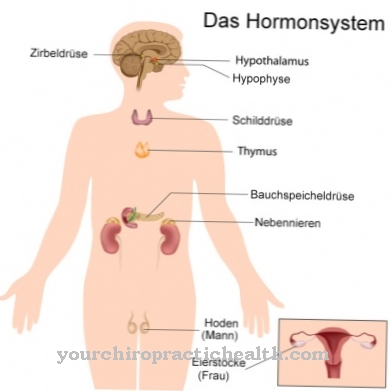
În acest scop, în organism există mecanisme de reglare hormonală. De exemplu, dacă prin alimente se consumă o mulțime de carbohidrați, nivelul zahărului din sânge crește. În același timp, este stimulată producția de insulină în pancreas.
Insulina furnizează celulelor glucoză. Acolo este fie defalcat pentru a genera energie sau, dacă necesarul de energie este scăzut, este transformat în acizi grași care pot fi depozitați sub formă de trigliceride (grăsimi) în țesutul adipos.
Dacă există o cantitate insuficientă de carbohidrați (foame, alimente extrem de scăzute de carbohidrați sau consum ridicat de glucoză în situații de urgență), nivelul de zahăr din sânge scade mai întâi. Aceasta numește antagonistul hormonal al insulinei, hormonul glucagon, la fața locului. Glucagonul determină glucogenul depozitat în ficat să se descompună în glucoză. Când aceste consumabile sunt consumate, gluconeogeneza crescută din aminoacizi pentru noua sinteză a glucozei începe în organism dacă faza foamei persistă.
Boli și afecțiuni
Dacă gluconoogeneza este perturbată, organismul poate avea glicemie scăzută (hipoglicemie). Hipoglicemia poate avea multe cauze. De exemplu, mecanismele de reglare hormonală duc la creșterea gluconeogenezei atunci când există o nevoie crescută de glucoză sau când se reduce aportul de carbohidrați.
Antagonistul hormonal al insulinei este hormonul glucagon. Când nivelul de zahăr din sânge scade, producția de glucagon crește, ceea ce determină apoi o gluconeogeneză crescută. În primul rând, glucogenul depozitat în ficat și mușchi este descompus și transformat în glucoză. Când se consumă toate rezervele de glucogen, aminoacizii glucogeni sunt convertiți în glucoză. Distrugerea mușchilor are loc pentru a furniza energie organismului.
Cu toate acestea, dacă gluconeogeneza este dificil de parcurs din diferite motive, apare hipoglicemie, care în cazuri severe poate duce la inconștiență și chiar la moarte.
De exemplu, bolile hepatice sau anumite medicamente pot împiedica gluconeogeneza. De asemenea, consumul de alcool inhibă gluconeogeneza. Hipoglicemia severă este o situație de urgență care necesită asistență medicală rapidă.
Un alt hormon care promovează gluconeogeneza este cortizolul. Cortizolul este un glucocorticoid care se găsește în cortexul suprarenal și acționează ca un hormon de stres. Sarcina sa este de a furniza rapid energia în situații fizice stresante. Pentru a face acest lucru, rezervele de energie fizică trebuie activate. Cortizolul stimulează conversia aminoacizilor din mușchii scheletului în glucoză ca parte a gluconeogenezei.
Dacă cortexul suprarenal este hiperactiv, de exemplu datorită unei tumori, se produce constant prea mult cortizol. Gluconeogeneza rulează apoi cu viteză maximă. Supraproducția de glucoză duce la ruperea mușchilor, o slăbire a sistemului imunitar și obezitatea trunchiului. Această imagine clinică este cunoscută sub numele de sindromul Cushing.











.jpg)