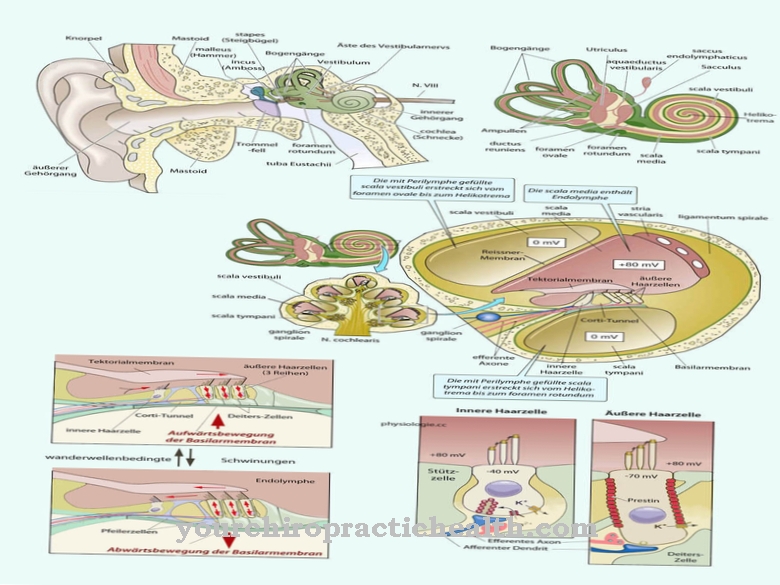
Legătură de hidrogen este o interacțiune între molecule care seamănă cu interacțiunile Van der Waals și are loc în corpul uman. Legătura joacă un rol în special în legătură cu legăturile peptidice și lanțurile de aminoacizi din proteine. Fără capacitatea de a se lega cu legăturile de hidrogen, un organism nu este viabil, deoarece îi lipsește aminoacizii vitali.
Ce este legătura de hidrogen?

Se numesc legături de hidrogen Legături de hidrogen sau H poduri abreviat. Este un efect chimic care se referă la interacțiunea atractivă a atomilor de hidrogen legați covalent cu perechi de electroni liberi ai unui atom de grupare. Interacțiunea se bazează pe polaritate și, descris mai precis, constă între atomii de hidrogen polarizați pozitiv într-o grupare amino sau hidroxil și perechi singulare de electroni din alte grupări funcționale.
Interacțiunea are loc numai în anumite circumstanțe. O condiție este proprietatea electronegativă a perechilor de electroni liberi. Această proprietate trebuie să fie mai puternică decât proprietatea electronegativă a hidrogenului pentru a crea o legătură puternică. Atomul de hidrogen poate fi astfel legat polar. De exemplu, atomii liberi electronici pot fi azot, oxigen și fluor.
Legăturile de hidrogen sunt legături de valență secundare, a căror rezistență este de obicei mult sub cea a legăturilor covalente sau a legăturilor ionice. Moleculele din legăturile de hidrogen au un punct de topire relativ ridicat și un punct de fierbere similar ridicat în raport cu masa lor molară. Legăturile au relevanță medicală în primul rând în raport cu peptidele și acizii nucleici din cadrul unui organism.
Legăturile de hidrogen sunt forțe intermoleculare. Fără existența lor, apa nu ar exista în diferite stări agregate, dar ar fi gazoasă.
Funcție și sarcină
Legatura de hidrogen are o interacțiune slabă și are loc între două particule sau în interiorul moleculelor. În acest context, tipul de legătură joacă un rol, de exemplu, în formarea structurilor terțiare în proteine. În biochimie, structură proteică înseamnă diferitele niveluri structurale ale unei proteine sau peptide. Structurile acestor substanțe naturale sunt împărțite ierarhic într-o structură primară, o structură secundară, o structură terțiară și o structură cuaternară.
Secvența de aminoacizi este structura primară. Ori de câte ori este menționată o proteină în legătură cu dispunerea sa spațială, se referă adesea la conformațiile proteice și la fenomenul schimbării conformaționale. În acest context, modificarea conformației corespunde unei modificări a structurii spațiale. Dispunerea proteinelor se bazează pe legătura peptidică. Acest tip de legătură conectează întotdeauna aminoacizii în același mod.
În celule, legăturile peptidice sunt mediate de ribozomi. Fiecare legătură peptidică corespunde unei conexiuni de grupări carboxilice ale unui aminoacid și grupări amino ale unui al doilea aminoacid, care este asociată cu eliminarea apei. Acest proces este cunoscut și sub denumirea de hidroliză.
În fiecare legătură peptidică, o singură legătură conectează o grupare C = O cu o grupare NH. Atomul de azot are exact o singură pereche de electroni. Din cauza electronegativității ridicate a oxigenului, această pereche liberă se află sub influența retragerii electronilor a atomilor de O2. În acest fel, oxigenul trage parțial perechea de electroni singulare în legătura dintre atomul de azot și atomul de carbon, iar legătura peptidică dobândește un caracter parțial de dublă legătură. Caracterul dublei legături elimină rotația liberă a grupelor NH și C = O.
Atomii de oxigen și atomii de hidrogen ai legăturilor peptidice sunt relevanți pentru formarea structurii tuturor peptidelor și proteinelor, fără excepție. În acest fel, doi aminoacizi se pot atașa între ei. După o astfel de atașare, toate legăturile peptidice ale două lanțuri de aminoacizi sunt direct opuse unul altuia. Atomii de hidrogen din legătura peptidică sunt relativ polarizați pozitiv în comparație cu atomii de oxigen din legăturile peptidice direct opuse. În acest fel, legăturile de hidrogen se formează și conectează cele două lanțuri de aminoacizi unul cu altul.
Toți aminoacizii din corpul uman sunt compuși organici alcătuiți din cel puțin o grupare carboxi și o grupă amino. Aminoacizii sunt o componentă structurală esențială a vieții umane. În plus față de a-aminoacizii proteinelor, sunt cunoscuți peste 400 de aminoacizi neproteogenici cu funcții biologice care nu ar putea apărea fără legătura de hidrogen. Forțele precum legătura de hidrogen stabilizează structura terțiară a aminoacizilor.
Vă puteți găsi medicamentul aici
➔ Medicamente pentru slăbiciune muscularăBoli și afecțiuni
Dacă există o tulburare în formarea structurilor spațiale proteinace funcționale, se vorbește de obicei despre tulburări de pliere a proteinelor. Una dintre aceste afecțiuni este boala Huntington. Această boală genetică este moștenită ca o trăsătură dominantă autosomală și se datorează unei mutații genetice în cromozomul 4. Mutația duce la instabilitatea produsului genic. Boala este o boală neurologică care este asociată în primul rând cu hiperkinezia involuntară a extremităților și feței distale. Hiperkineza persistentă duce la rigiditatea mușchilor afectați. În plus, pacienții cu boala suferă de un consum crescut de energie.
Simptomele patologice în legătură cu legăturile de hidrogen sau cu structura generală de proteine sunt, de asemenea, prezente în bolile prionice, precum boala vacilor nebune. Cea mai populară ipoteză este că BVB induce o pliere greșită a proteinelor. Aceste proteine pliate greșit nu pot fi defalcate prin procese fiziologice și, prin urmare, se acumulează în țesut, în special în sistemul nervos central. Rezultatul este degenerarea celulelor nervoase.
Malformațiile structurii proteice sunt de asemenea discutate în legătura cauzală a bolii Alzheimer. Bolile menționate nu afectează în mod direct legătura de hidrogen, ci se referă la structura spațială a proteinelor, la care legătura de hidrogen contribuie semnificativ.
Un organism cu o incapacitate absolută de legătură cu hidrogen nu este viabil. O mutație care cauzează acest lucru ar duce la un avort în sarcina timpurie.










.jpg)





.jpg)