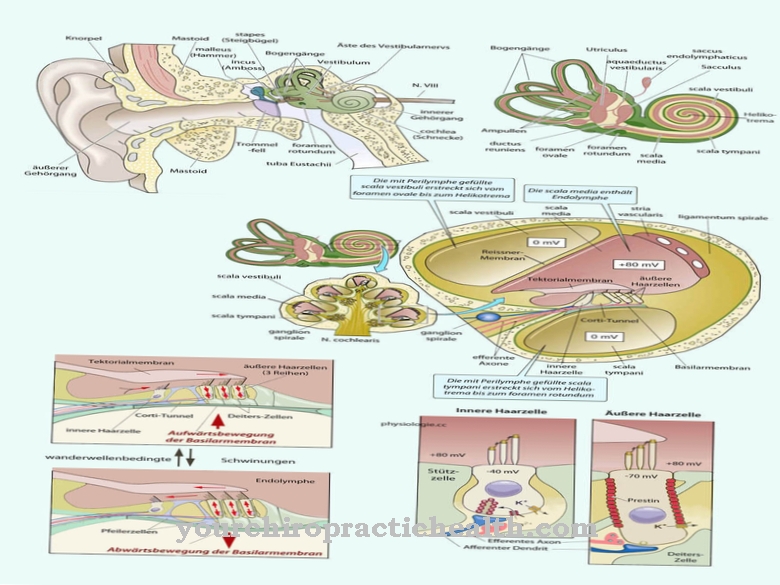
Lipitură reprezintă un proces crucial în timpul transcrierii în nucleul eucariotei, în timpul căruia mRNA-ul matur apare din pre-mARN. Intronii care sunt încă conținuți în ARNm pre-transcriere după transcriere sunt îndepărtați și exonii rămași sunt combinați pentru a forma ARNm finalizat.
Ceea ce este splicing

Dogma centrală a biologiei moleculare afirmă că fluxul de informații genetice are loc de la ADN-ul purtător de informații prin ARN la proteină. Primul pas în exprimarea genelor este ceea ce este cunoscut sub numele de transcriere. ARN este sintetizat folosind ADN-ul ca șablon. ADN-ul este purtătorul informațiilor genetice, care sunt stocate acolo cu ajutorul unui cod format din cele patru baze adene, timină, guanină și citozină. Complexul proteic ARN polimerază citește secvența de bază a ADN-ului în timpul transcrierii și produce „ARN-ul mesagerului” corespunzător (pre-ARNm pentru scurt). În loc de timină, uracilul este întotdeauna încorporat.
Genele sunt formate din exoni și introni. Exonii sunt acele părți ale genomului care codifică de fapt informațiile genetice. În schimb, intronii reprezintă secțiuni care nu codifică în cadrul unei gene.Genele stocate pe ADN sunt traversate de secțiuni lungi care nu corespund niciunui aminoacizi din proteina ulterioară și nu contribuie la traducere.
O genă poate avea până la 60 de introni, cu lungimi cuprinse între 35 și 100.000 de nucleotide. În medie, acești introni sunt de zece ori mai lungi decât exonii. Pre-mRNA produs în prima etapă a transcrierii, de asemenea adesea denumit ARNm imatur, conține încă atât exoni, cât și introni. Aici începe procesul de împletire.
Intronii trebuie eliminați din pre-mARN și exonii rămași trebuie legați între ei. Numai atunci mRNA matur poate părăsi nucleul celular și poate iniția traducerea.
Splicingul este efectuat în cea mai mare parte cu ajutorul spliceozomului (germană: spliceosome). Acesta este format din cinci snRNP (particule mici de ribonucleoproteine nucleare). Fiecare dintre aceste snRNP-uri constă dintr-un snRNA și proteine. Unele alte proteine care nu fac parte din snRNP-uri fac parte și din spliceozom. Spliceozomii sunt împărțiți în spliceozomi majori și minori. Spliceozomul major procesează peste 95% din totalul intronilor umani, spliceozomul minor se ocupă în principal de intronii ATAC.
Pentru explicația splicing-ului, Richard John Roberts și Phillip A. Sharp au primit premiul Nobel pentru medicină în 1993. Thomas R. Cech și Sidney Altman au primit premiul Nobel pentru chimie în 1989 pentru cercetările lor asupra splicing-ului alternativ și efectul catalitic al ARN.
Funcție și sarcină
În timpul procesului de împletire, spliceozomul este format din nou din părțile sale individuale. La mamifere, snRNP U1 se atașează mai întâi la locul 5-splice și inițiază formarea spliceosomului rămas. SnRNP U2 se leagă de punctul de ramificare al intronului. Prin urmare, se leagă, de asemenea, tri-snRNP.
Spliceozomul catalizează reacția de splicing prin intermediul a două transesterificări succesive. În prima parte a reacției, un atom de oxigen din grupa 2’-OH a unei adenozine din „secvența punctului de ramură” (BPS) atacă un atom de fosfor al unei legături de fosfodiester în situsul 5’-splice. Aceasta eliberează exonul de 5 'și circulă intronul. Atomul de oxigen al grupului 3’-OH acum liber al exonului 5’ se leagă acum la locul 3-splice, prin care cei doi exoni sunt conectați și intronul este eliberat. Intronul este adus într-o conformație simplificată, numită lariat, care este apoi defalcată.
Spre deosebire de aceasta, spliceozomii nu joacă un rol în auto-splicing. Aici intronii sunt excluși din traducere prin structura secundară a ARN-ului în sine. Splicingul enzimatic al ARNt (ARN de transfer) apare la eucariote și arhee, dar nu și în bacterii.
Procesul de splicing trebuie să se desfășoare cu o precizie extremă exact la limita exon-intronului, deoarece o abatere de la o singură nucleotidă ar duce la codificarea incorectă a aminoacizilor și, astfel, la formarea de proteine complet diferite.
Splicing-ul unui pre-mRNA se poate dovedi diferit datorită influențelor de mediu sau tipului de țesut. Aceasta înseamnă că diferite proteine pot fi formate din aceeași secvență ADN și, așadar, același pre-mARN. Acest proces este cunoscut sub numele de splicing alternativ. O celulă umană conține în jur de 20.000 de gene, dar este capabilă să producă câteva sute de mii de proteine datorită splicing-ului alternativ. Aproximativ 30% din toate genele umane au splicing alternativ.
Splicingul a jucat un rol major în evoluție. Exonii codează adesea domenii individuale ale proteinelor, care pot fi combinate între ele în moduri diferite. Aceasta înseamnă că din doar câțiva exoni pot fi produse o mare varietate de proteine cu funcții complet diferite. Acest proces se numește amestecarea exonului.
Boli și afecțiuni
Unele boli ereditare pot fi strâns legate de splicing. Mutațiile intronilor care nu codifică de obicei nu conduc la erori în formarea proteinelor. Cu toate acestea, dacă o mutație are loc într-o parte a unui intron care este importantă pentru reglarea splicing-ului, aceasta poate duce la splicarea defectuoasă a pre-mARN. ARNm matur rezultat apoi codifică proteine defectuoase sau, în cel mai rău caz, proteine dăunătoare. Acesta este cazul, de exemplu, cu unele tipuri de beta-talasemie, o anemie moștenită. Alți reprezentanți ai bolilor care se dezvoltă în acest fel sunt, de exemplu, sindromul Ehlers-Danlos (EDS) de tip II și atrofia musculară spinală.







.jpg)





.jpg)